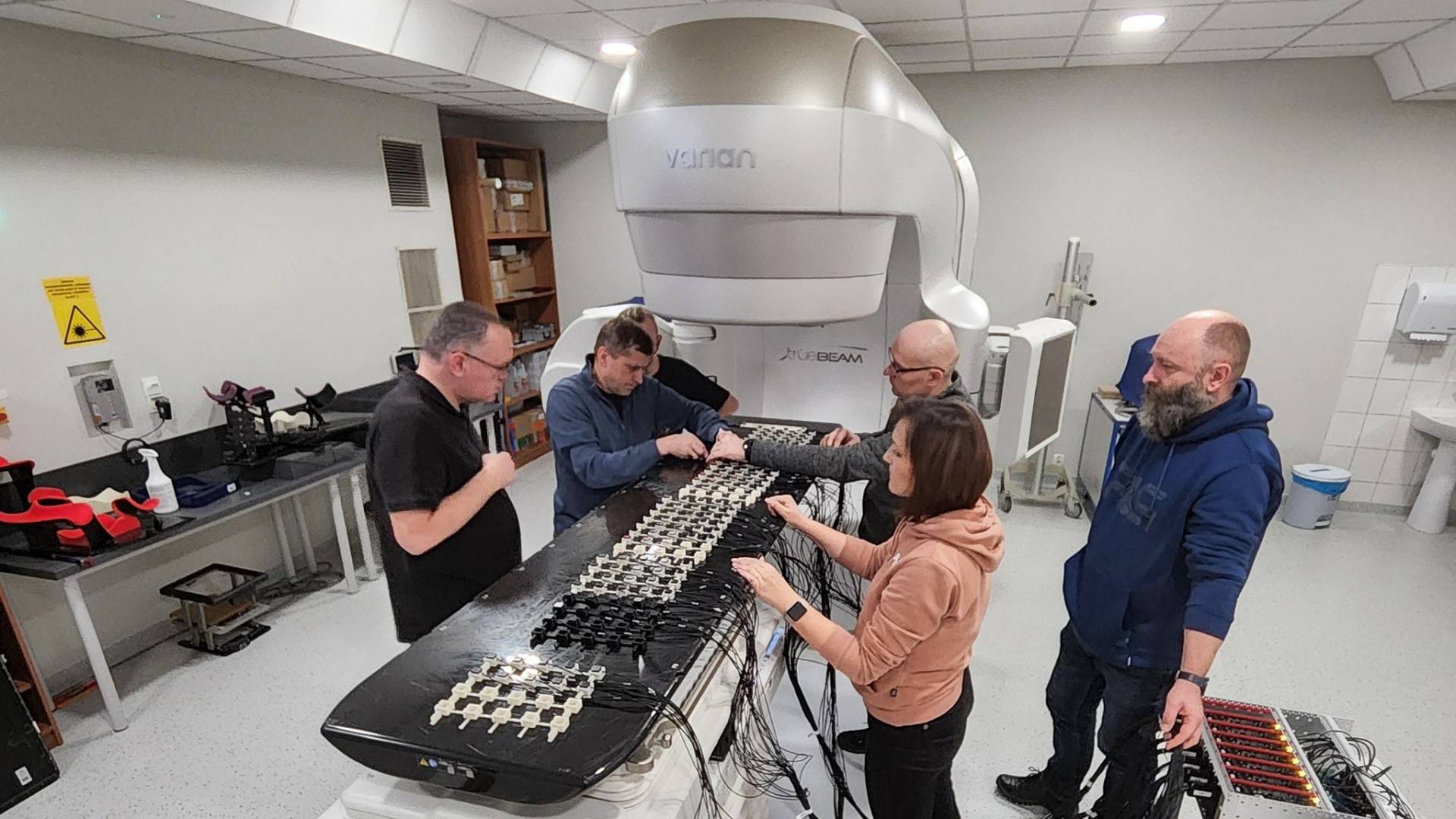
Krakowscy naukowcy zbudowali urządzenie, dzięki któremu można będzie sprawdzić dawkę promieniowania przez podaniem jej pacjentowi, żeby poprawić w ten sposób efektywność i dokładność radioterapii w leczeniu raka. “Raz wyemitowanej dawki promieniowania nie możemy już cofnąć. Ale co gdybyśmy byli w stanie dokładnie zobaczyć jej działanie, zanim dotrze ona do ciała pacjenta?” - zastanawiają się badacze.
Reklama
Prototyp detektora jest już gotowy, teraz przed nim etap wprowadzenia do użycia. Projekt Dose - 3D, w ramach którego naukowcy stworzyli urządzenie, powstał po to, by w przyszłości dawki promieniowania dało się testować wielokrotnie, na fantomie.
“Dzięki temu fizycy i lekarze mieliby pewność, że stosują optymalny plan leczenia” - wyjaśniają badacze i precyzują, że w ten sposób medycy będą mogli stworzyć plan leczenia identyczny, jak dla pacjenta, dokładnie zmierzyć, jaka jest dawka promieniowania w miejscu, które reprezentuje w fantomie jakąś zmianę chorobową i jaki jest jej rozkład przestrzenny.
Dose - 3D został zainicjowany przez Akademię Górniczo - Hutniczą, Politechnikę Krakowską i Narodowy Instytut Onkologii w Krakowie. Dalsze prace badawczo - rozwojowe kontynuowane są przez zespół z AGH i eksperta z NIO. Kierownik projektu, prof. Tomasz Szumlak z Katedry Oddziaływań i Detekcji Cząstek na Wydziale Fizyki i Informatyki Stosowanej AGH przyznaje, że inspiracją do rozpoczęcia projektu Dose-3D było marzenie fizyka medycznego o narzędziu, które pozwoliłoby na sprawdzenie dawki promieniowania przed podaniem jej pacjentowi.
“Jeden z medyków powiedział, że takim super urządzeniem byłby detektor, który mierzyłby dawkę promieniowania w jednym momencie w całej objętości modelowanej i od razu w czasie rzeczywistym dostarczał informacje na temat zdeponowanej dawki terapeutycznej. Ta szybka myśl przerodziła się w serię dyskusji z ekspertami z Narodowego Instytutu Onkologii i Politechniki Krakowskiej, co w efekcie zaowocowało pozyskaniem, w ramach projektu Team-NET Fundacji na Rzecz Nauki Polskiej, funduszy europejskich z Programu Operacyjnego Inteligentny Rozwój”. Teraz naukowcy z AGH współpracują także z Instytutem Fizyki Jądrowej, żeby przetestować swój detektor przy użyciu wiązki protonowej.
“Pacjenci oczywiście są bezpieczni, ale przydałoby się takie urządzenie jak nasz fantom, żeby bezpośrednio zmierzyć wiązkę promieniowania w zadanej objętości. Teoretycznie dzięki takiemu rozwiązaniu moglibyśmy mieć dostęp do informacji o tym, jak dokładnie wygląda pęczek tych protonów. Są z tym oczywiście problemy, bo taka wiązka protonowa jest jednak potężna, w sensie możliwej do zdeponowania energii jest jak… pociąg. I „wjeżdżając” do tego detektora potencjalnie mogłaby dokonać zniszczeń albo wywołać efekt tzw. quenchingu jonizacyjnego tej wiązki. To niepożądane zjawisko, które może występować w systemach detekcji promieniowania, gdy mamy do czynienia z wysoko jonizującym promieniowaniem, jakim jest też wiązka protonowa. Mówimy o nim, gdy odpowiedź detektora na zdeponowaną energię jest nieliniowa. Tymczasem pożądaną cechą systemów detekcji promieniowania jest właśnie liniowość odpowiedzi. Quenching jonizacyjny jest więc efektem bardzo istotnym, ale z naszej perspektywy niekorzystnym”.
Reklama
W rozmowie z Katarzyną Dziadowicz z Centrum Komunikacji i Marketingu AGH, opublikowanej na stronie internetowej uczelni, fizyk zaznacza również, opracowany przez jego zespół detektor ma mieć zastosowanie w terapii fotonowej. Radioterapia z użyciem wiązek fotonowych jest jednym ze sposobów leczenia onkologicznego. W odróżnieniu od terapii protonowej może być stosowana do bardzo rozległych zmian nowotworowych o skomplikowanych kształtach, umiejscowionych w różnych częściach ciała. Istotną różnicą pomiędzy terapią fotonową i protonową jest sposób dostarczania dawki terapeutycznej, która efektywnie niszczy tkanki nowotworowe.
“W przypadku protonów jonizacja jest mniej więcej stała, a w momencie utraty znacznej części energii kinetycznej protony gwałtownie tracą energię, to tak zwane maksimum Bragga. Dzięki temu terapia protonowa może być stosowana w przypadku nowotworów umiejscowionych płytko, mówiąc w znacznym uproszczeniu”. Problem pojawia się wtedy, gdy zmiana nowotworowa jest rozległa i głęboko umiejscowiona, jak w przypadku tkanek miękkich, takich jak płuca.
“Tu zaczyna się problem dla terapii protonowej, bo wtedy proces jonizacji dotyka też tej zdrowej tkanki „po drodze” i jest dosyć intensywny, bo wiązka ją penetruje, żeby dotrzeć na taką głębokość. Dlatego jeśli mamy rozległe zmiany chorobowe i one są głęboko, to kierujemy się ku terapii fotonowej”.
Zespół, który pracuje nad badaniami prototypu, tworzą naukowcy: Bartosz Mindur, Piotr Wiącek, Jakub Hajduga, Tomasz Szumlak, Dagmara Kulig i Damian Kabat.